WordPress 網站
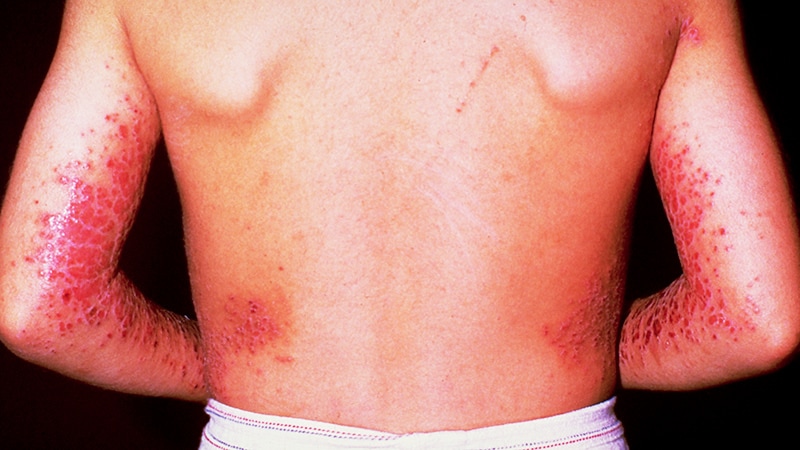
美國食品藥物管理局(FDA)已批准白介細胞素(IL)-13產品lebrikizumab (Ebglyss)用於治療中度至重度異位性皮膚炎(AD)的成人和12歲及以上兒童雖然採用局部處方治療進行治療,但仍無法得到良好的控制。
注射藥物候選者的體重必須至少為 88 磅(40 公斤);lebrikizumab 的建議初始起始劑量包括在基線和第 2 週注射 500 mg(兩次 250 mg 注射),然後每 2 週注射 250 mg,直到第16週或之後達到足夠的臨床反應。
根據一直在開發lebrikizumab的禮來公司的新聞稿,該批准是基於ADvocate 1、ADvocate 2和ADhere研究的結果,該研究納入了1000多個標準中度至重度AD的成人和12歲及以上兒童。
據禮來公司稱,服用lebrikizumab的ADvocate 1和2中,有38%的人在16週時獲得了透明或幾乎透明的皮膚,而實驗組中這一比例為12%,而10%早在4週時就出現了這些結果。稱,平均而言,服用lebrikizumab 的患者在第16 週時搔癢得到緩解,佔43%,而服用lebrikizumab 的患者中這一比例為12%。
臨床試驗中觀察到lebrikizumab最常見的副作用包括眼睛和眼瞼炎症,如發紅、腫脹和搔癢;注射部位反應;和帶狀皰疹。
Lebrikizumab於2024年1月在日本獲得批准,並於2023年獲得歐盟委員會批准。